A decisão foi divulgada nesta quinta-feira (16) após avaliação técnica do pedido submetido pela farmacêutica no dia 12 de novembro
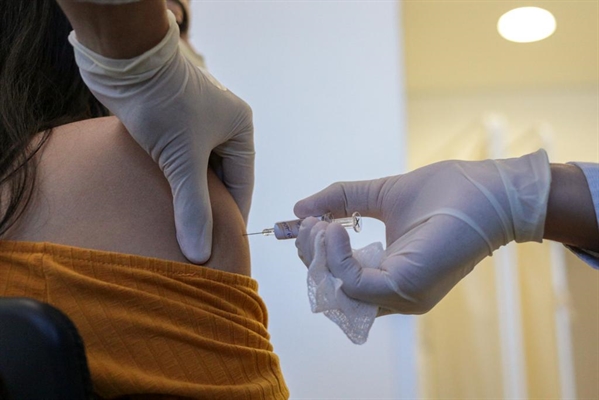
A decisão foi divulgada nesta quinta-feira (16) após avaliação técnica (Foto: Governo do Estado de São Paulo)
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou o uso da vacina da Pfizer contra a Covid-19 em crianças de 5 a 11 anos de idade no Brasil. A decisão foi divulgada nesta quinta-feira (16) após avaliação técnica do pedido submetido pela farmacêutica no dia 12 de novembro.
A dosagem da vacina para esta faixa etária será ajustada e menor (um terço) que aquela utilizada por maiores de 12 anos. Segundo a Anvisa, a proposta é ter frascos diferentes, com dosagem específica para cada grupo. Os frascos serão diferenciados pela cor, roxa para adultos e adolescentes e laranja para crianças, de acordo com a Pfizer.
Na reunião pública transmitida ao vivo pela Anvisa, o diretor-geral de Medicamentos da agência, Gustavo Mendes, afirmou que as evidências científicas disponíveis apontam que a vacina administrada no esquema de duas doses para crianças de 5 a 11 anos pode ser eficaz na prevenção de doença grave e de óbitos.
O início da campanha de imunização de crianças será definido pelo Ministério da Saúde, ainda sem previsão de data. As doses para uso pediátrico ainda não estão disponíveis no país.
O passo a passo até a aprovação
No dia 9 de novembro, especialistas da Anvisa e da Pfizer realizaram uma reunião de pré-submissão do pedido de indicação da vacina para crianças de 5 a 11 anos. No encontro, foram apresentados dados técnicos antes do envio formal do pedido.
A Anvisa recebeu o pedido da farmacêutica no dia 12 de novembro, quando deu início à análise técnica.
No dia 23 de novembro, a Anvisa solicitou à Pfizer a apresentação de dados adicionais para a avaliação do pedido. O pacote de informações em resposta às exigências da agência foram entregues no dia 6 de dezembro.
No dia 3 de dezembro, a Anvisa realizou uma reunião com um grupo de especialistas em imunologia e pediatria que estão acompanhando a análise das vacinas.
A autorização do uso da vacina da Pfizer em crianças de 5 a 11 anos de idade foi emitida no dia 16 de dezembro, após a finalização da análise pela equipe técnica da Anvisa.
A decisão contou com a participação de representantes de sociedades médicas brasileiras, incluindo a Sociedade Brasileira de Infectologia (SBI), a Sociedade Brasileira de Pneumologia e Tisiologia (SBPT), a Sociedade Brasileira de Pediatria (SBP) e a Sociedade Brasileira de Imunizações (SBIm).
Uso da Pfizer no Brasil
A vacina da Pfizer é um dos quatro imunizantes contra a Covid-19 aplicados no Brasil, além da AstraZeneca, Coronavac e Janssen – sendo o único com autorização para uso em crianças e adolescentes.
A vacina está registrada no país desde 23 de fevereiro. No registro inicial estavam contemplados indivíduos com mais de 16 anos. No dia 11 de junho, a Anvisa autorizou a inclusão da faixa etária de 12 a 15 anos.
Como funcionam os pedidos de inclusão de faixas etárias
Para que uma nova faixa etária seja incluída na indicação da bula de uma vacina no Brasil, o laboratório produtor do imunizante deve realizar a solicitação junto à Anvisa.
O laboratório precisa conduzir e apresentar estudos que demonstrem a relação de segurança e eficácia da vacina para esta nova faixa etária.
De acordo com a Anvisa, os principais pontos de atenção em relação ao público infantil são os dados de segurança e eventos adversos identificados, ajustes de dosagem da vacina e fatores específicos dos organismos das crianças em fase de desenvolvimento.
O prazo de avaliação da solicitação pela Anvisa é de até 30 dias.
Uso da Pfizer em crianças é autorizado nos Estados Unidos e Europa
O uso emergencial da vacina da Pfizer em crianças de 5 a 11 anos nos Estados Unidos foi autorizado pelo Food and Drug Administration (FDA), órgão semelhante à Anvisa, no dia 29 de outubro.
A decisão ocorreu após a votação, por unanimidade, dos conselheiros do FDA, pela recomendação da utilização da vacina formulada com um terço da dose utilizada em pessoas maiores de 12 anos.
A Agência Europeia de Medicamentos (EMA, na sigla em inglês) também aprovou o uso do imunizante contra a Covid-19 em crianças. A decisão foi divulgada no dia 25 de novembro.
“Os efeitos adversos mais frequentes em crianças dos 5 aos 11 anos são semelhantes aos das pessoas com 12 anos ou mais. Incluem dor no local da injeção, cansaço, dor de cabeça, vermelhidão e inchaço no local da injeção, dores musculares e calafrios. Esses efeitos são geralmente leves ou moderados e melhoram alguns dias após a vacinação”, diz o comunicado da agência europeia.
Anvisa avalia segundo pedido do Butantan
A Anvisa avalia um segundo pedido do Instituto Butantan para a indicação da Coronavac para crianças e adolescentes de 3 a 17 anos. O pedido foi recebido na quarta-feira (15) e tem prazo para avaliação de 30 dias.
O primeiro pedido apresentado pelo Butantan para utilização do imunizante nesta faixa etária foi realizado em julho. A autorização foi rejeitada pela Anvisa no dia 18 de agosto pela limitação de dados dos estudos apresentados naquele momento, segundo a agência.
Diretores da Anvisa recebem ameaças
No dia 28 de outubro, cinco diretores da Anvisa receberam ameaças de morte por e-mail caso houvesse aprovação pela agência de vacinas contra a Covid-19 para crianças. No dia seguinte, uma segunda correspondência eletrônica, desta vez anônima, fez ameaças a servidores, diretores, funcionários terceirizados e seus familiares.
Diante das ameaças, a Anvisa acionou a Polícia Federal para investigações. No dia 5 de novembro, a Polícia Civil do Paraná afirmou ter identificado o homem que ameaçou autoridades do estado do Paraná e da Anvisa. O nome do suspeito não foi revelado.
**Com CNN Brasil










